O Que É Doença De Chagas? Como É Transmitida?

Os sintomas mudam ao longo do curso da infecção. Na fase inicial, eles podem não estar presentes ou podem ser: febre, gânglios linfáticos aumentados, dor de cabeça e inchaço no local da mordida. Após 8-12 semanas, os indivíduos entram na fase crônica da doença e em 60-70% nunca desenvolvem outros sintomas.
Os 30 a 40% restantes apresentam sintomas adicionais de 10 a 30 anos após a infecção inicial. Isto inclui o alargamento dos ventrículos do coração em 20 a 30% levando a insuficiência cardíaca. A dilatação do esôfago ou o alargamento do cólon também podem ocorrer em 10% das pessoas.
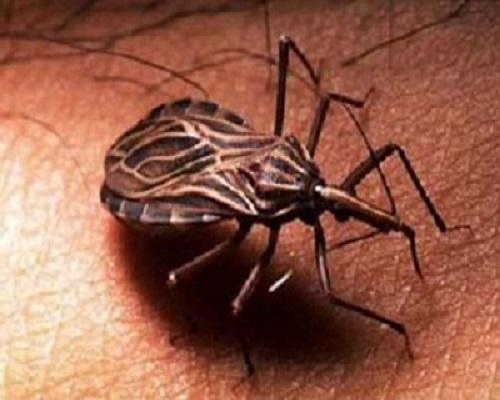
T. cruzi é transmitido para humanos e outros mamíferos principalmente pela via vetorial, através da picada de insetos hematófagos da subfamília Triatominae, popularmente denominados de "barbeiros".
A doença pode também ser transmitida através de transfusão de sangue, transplante de órgãos, ingestão de alimentos contaminados com o parasita e da mãe para o feto. O diagnóstico precoce da doença é feito pela detecção do parasita no sangue, utilizando um microscópio. A forma crônica é diagnosticada pela presença de anticorpos para T. cruzi no sangue.
A prevenção ocorre principalmente pela eliminação dos barbeiros e em evitar suas picadas. Outros esforços de prevenção incluem a triagem do sangue usado para transfusões. Infecções precoces são tratáveis com a medicação benznidazol ou nifurtimox.
Eles quase sempre resultam em cura se forem dados no início, no entanto, tornam-se menos eficazes quanto mais tempo se passa após contrair a doença. Quando utilizados na forma crônica podem retardar ou prevenir o desenvolvimento de sintomas em fase terminal.
Benznidazol e nifurtimox causam efeitos colaterais temporários em até 40% das pessoas, incluindo doenças de pele, toxicidade cerebral e irritação do sistema digestório.
Estima-se que 7 000 000-8 000 000 pessoas, sobretudo no México, América Central e América do Sul, têm a doença de Chagas. Isso resulta em cerca de 12 500 mortes por ano desde 2006. A maioria das pessoas com a doença são indivíduos de baixa renda e grande parte das pessoas com a doença não percebem que estão infectadas.
Movimentos populacionais em grande escala têm expandido as áreas onde os casos da doença de Chagas são encontrados e estes passaram a incluir muitos países da Europa e nos Estados Unidos. Essas áreas também têm visto um aumento nos casos até 2014.
A doença foi descrita pela primeira vez em 1909 por Carlos Chagas do qual recebeu o nome. Ela afeta mais de 150 outras espécie de animais.
Nas áreas endêmicas, o principal mecanismo de transmissão é o vetorial, ou seja, através de um inseto vetor da subfamília Triatominae,2 principalmente dos gêneros Triatoma, Rhodnius e Panstrongylus.3 O inseto infecta-se com Trypanosoma cruzi ao alimentar-se de sangue de animais ou humanos contaminados.
De hábitos noturnos, ele esconde-se durante o dia em fendas nas paredes e telhados, e emerge à noite, quando os habitantes estão dormindo. Por causa da tendência de picar a face das pessoas, o inseto é popularmente conhecido como "barbeiro" ou "chupão". Após a picada e a ingestão de sangue, ele defeca próximo ao local.
O prurido intenso no local da picada ajuda as formas infectantes de T. cruzi (denominadas de tripomastigotas), nas fezes, a penetrarem na ferida da picadura, mas elas também podem penetrar por mucosas intactas, como a conjuntival.2
Uma vez dentro do hospedeiro, o tripomastigota invade as células próximas à inoculação, onde diferenciam-se em amastigotas intracelulares.
Os amastigotas multiplicam-se por divisão binária e diferenciam-se em tripomastigotas, que são liberados na corrente sanguínea, infectando células de tecidos variados, e este ciclo então é repetido diversas vezes. As manifestações clínicas são resultado deste ciclo infeccioso. Os tripomastigotas circulantes não se replicam (diferente da tripanossomíase africana). E a replicação só recomeça quando os parasitas entram em outras células ou são ingeridos por outro vetor.2
Como doença caracteristicamente rural, tradicionalmente acomete pessoas de origem interiorana que habitam ou habitaram casas de baixa qualidade, onde o vetor facilmente se aloja e coloniza.4 Vegetação densa (como as das florestas tropicais) e habitats urbanos não são ideais para o estabelecimento do ciclo de transmissão humano.
No entanto, em regiões onde o habitat silvestre e sua fauna são reduzidos pela exploração econômica e ocupação humana, como em áreas recém desmatadas, áreas de cultura da Leopoldinia piassaba, e algumas partes da região amazônica, um ciclo de transmissão humano pode desenvolver-se quando os insetos procuram por novas fontes de alimentação.5
T. cruzi pode também ser transmitido por transfusões de sangue. Com a exceção dos derivados sanguíneos (como anticorpos fracionados), todos os componentes do sangue são infecciosos. O parasita permanece viável a 4 °C por até no mínimo 18 dias ou mais de 250 dias quando mantido em temperatura ambiente. Não está claro se o T. cruzi pode ser transmitido por meio de componentes do sangue congelados e descongelados.6
Outros modos de transmissão incluem o transplante de órgãos, amamentação e por exposição laboratorial acidental.7 A doença de Chagas também pode ser passada de uma mulher grávida para seu filho (transmissão congênita) através da placenta, com uma prevalência entre as gestantes na América do Sul de 4 a 64,4%, com 0,1 a 7% destas mulheres transmitindo a infecção para os fetos.
Essa forma de transmissão constitui um problema em ascensão na saúde pública e é uma das responsáveis pela urbanização dos casos e pela disseminação da doença em áreas não endêmicas.8
A transmissão oral é uma via pouco frequente de infecção, mas tem sido descrita. Em 1991, trabalhadores rurais no estado da Paraíba, Brasil, foram infectados ao ingerir comida contaminada; transmissão também foi documentada pela ingestão de suco de açaí e caldo de cana infectados.9 10 11 12 13 Um surto em 2007 em 103 crianças numa escola na Venezuela foi atribuído a contaminação do suco de guava.
A doença de Chagas é um problema emergente na Europa, por causa da grande maioria dos casos de infecção crônica serem assintomáticos e por causa de migrantes provenientes da América Latina.
A doença apresenta dois estágios em seres humanos: uma fase aguda, que ocorre pouco tempo após a infecção, e uma fase crônica que se desenvolve ao longo de muitos anos.
A fase aguda ocorre durante as primeiras semanas ou meses desde a infecção. Geralmente, ela não é notada por ser assintomática ou por exibir apenas sintomas moderados que não são únicos da doença de Chagas. Os sintomas podem incluir febre, fadiga, dor no corpo, dor de cabeça, exantema, perda de apetite, diarreia e vômitos. Os sinais no exame físico podem incluir aumento moderado do fígado, do baço e de linfonodos, e inchaço no local da picada do barbeiro (o chagoma).
O marcador mais conhecido da fase aguda da doença de Chagas é chamado sinal de Romaña. O sinal é caracterizado pelo edema das pálpebras do mesmo lado do rosto em que se localiza a ferida produzida pela picada do barbeiro, onde as fezes foram depositadas pelo inseto ou mesmo quando acidentalmente esfregadas para dentro do olho.
Raramente, crianças e adultos morrem durante a fase aguda da doença, porém pode ocorrer uma grave inflamação do músculo cardíaco (miocardite) ou do cérebro (meningoencefalite), que colocam a vida em risco.16 A fase aguda também pode ser grave em pessoas com o sistema imunitário comprometido.
Se houver o desenvolvimento de sintomas durante a fase aguda, eles geralmente se resolvem espontaneamente dentro de três a oito semanas em aproximadamente 90% dos indivíduos.17 18 Embora os sintomas se resolvam, mesmo com o tratamento, a infecção persiste e entra em sua fase crônica.
Dos indivíduos com doença de Chagas crônica, 60–80% jamais desenvolverão sintomas (chamada doença de Chagas crônica indeterminada), enquanto 20–40% desenvolverão sintomas cardíacos e/ou problemas digestivos (chamada doença de Chagas crônica determinada).
Em 10% dos indivíduos, a doença progride diretamente da fase aguda para uma forma clínica sintomática da doença de Chagas.17 18
A doença crônica sintomática (determinada) afeta vários sistemas do organismo, como nervoso, digestório e cardíaco. Cerca de dois terços das pessoas com sintomas crônicos apresentam danos ao coração, incluindo a miocardiopatia dilatada, que causa anormalidades do ritmo cardíaco e pode resultar em morte súbita. Cerca de um terço dos pacientes apresenta danos ao sistema digestório, resultando em dilatação do trato digestivo (megacólon e megaesôfago), acompanhados de grave emagrecimento.
A dificuldade de deglutição (secundária à acalásia) pode ser o primeiro sintoma dos distúrbios digestivos e pode levar à desnutrição.
20% a 50% dos indivíduos com envolvimento intestinal também exibem acometimento cardíaco. Mais de 10% das pessoas cronicamente infectadas desenvolvem neurite, que resulta em alterações sensoriais e dos reflexos tendinosos.
Casos isolados exibem envolvimento do sistema nervoso central, incluindo demência, confusão, encefalopatia crônica e perdas sensoriais e motoras.20
As manifestações clínicas da doença de Chagas se devem à morte de células nos tecidos envolvidos no ciclo infeccioso do parasita, induzindo a respostas inflamatórias, lesões celulares e fibrose.
Por exemplo, o amastigoto intracelular destrói os neurônios intramurais do sistema nervoso autônomo do intestino e do coração, levando ao megacólon e aos aneurismas cardíacos, respectivamente. Se não tratada, a doença de Chagas pode ser fatal, na maioria dos casos por danificação do tecido muscular cardíaco.19
Há uma considerável variação geográfica na ocorrência das complicações cardíacas e de dilatações gastrointestinais em pacientes com doença de Chagas crônica.
Na maioria dos países da América do Sul, as dilatações são quase tão comuns quanto o comprometimento cardíaco. Mas na Colômbia, Venezuela, América Central e México as dilatações são praticamente desconhecidas. Não se sabe se fatores do hospedeiro ou diferenças nas cepas do parasita causariam estes diferentes padrões de expressão clínica da doença
Na fase aguda, a presença do T. cruzi é diagnóstica para a doença de Chagas. Essa fase é caracterizada pela alta parasitemia, o que permite um diagnóstico parasitológico.21 O parasita, em sua forma móvel (tripomastigota), pode ser detectado por exame microscópico direto no esfregaço de sangue fresco ou da camada leucocitária; ou pela preparação de esfregaços corados com Giemsa ou Leishman.4 Microscopicamente, o T. cruzi pode ser confundido com o Trypanosoma rangeli, que não é patogênico para humanos.22 O T. cruzi pode também ser isolado por cultura em meios específicos (por exemplo NNN, LIT), tanto na fase aguda como na crônica.
A fase crônica da enfermidade é caracterizada pela baixa parasitemia e alto nível de anticorpos, diminuindo a eficiência da identificação direta do parasita. Portanto, outros métodos são empregados durante esta fase, entre eles a hemoaglutinação indireta (IFA), imunoflurescência indireta (IIF), enzyme-linked immunosorbent assay (ELISA), quimioluminescência, TESA-blot, reação em cadeia da polimerase (PCR) e pelo xenodiagnóstico,onde percevejos não infectados são alimentados com o sangue do paciente suspeito, e então seus intestinos são examinados para a detecção do parasita.
Atualmente, ainda não existe uma vacina contra a doença de Chagas26 e a prevenção é, em geral, focada em eliminar o inseto vetor com a utilização de sprays e tintas contendo inseticidas (piretroides sintéticos), e em melhorar as condições de saneamento e habitação nas áreas rurais.
Para os moradores de áreas urbanas que vão passar temporadas, como férias ou acampamentos, em regiões endêmicas, recomenda-se o uso de mosquiteiros. Algumas medidas de controle incluem:
Uma armadilha contendo uma levedura pode ser utilizada para monitorar infestações de certas espécies de triatomíneos (Triatoma sordida, Triatoma brasiliensis, Triatoma pseudomaculata e Panstrongylus megistus).
Foram apresentados resultados promissores com o tratamento dos habitats de vetores com o fungo Beauveria bassiana.
Pode-se selecionar simbiontes do Triatominae através de paratransgênese. Inúmeras vacinas estão sendo testadas atualmente. A vacinação com o Trypanosoma rangeli tem produzido resultados positivos em modelos animais.
Mais recentemente, o potencial de vacinas com DNA para imunoterapia da doença de Chagas nas fases aguda e crônica tem sido testado por vários grupos de pesquisadores.32
Antigamente, a transfusão de sangue era o segundo modo mais comum de transmissão da doença de Chagas, mas, com o desenvolvimento e a implementação do controle dos bancos de sangue, houve uma redução dramática desse risco na última década.
A doação de sangue em todos os países endêmicos da América Latina é submetida a uma pesquisa para Chagas. O teste está sendo expandido para outros países, como França, Espanha e Estados Unidos, que apresentam populações significativas ou em crescimento de imigrantes oriundos de áreas endêmicas.
Na Espanha, os doadores são avaliados com questionários para identificar indivíduos em risco de exposição à doença de Chagas para realizar a triagem.
O Food and Drug Administration (FDA), órgão responsável pela aprovação de medicamentos nos EUA, aprovou dois testes para Chagas e publicou manuais que recomendam a triagem de qualquer sangue ou tecido doados.
Apesar de esses testes não serem obrigatórios nos EUA, estima-se que atualmente 75-90% das doações são testadas para Chagas, incluindo todas as unidades coletadas pela Cruz Vermelha Americana, o que corresponde a 40% de todo o suprimento sanguíneo do país.
O Chagas Biovigilance Network relata a incidência atual de produtos sanguíneos positivos para Chagas nos Estados Unidos, segundo o que é notificado pelos laboratórios utilizando os testes de rastreio aprovados pelo FDA em 2007.
Na doença de Chagas, o tratamento é baseado em drogas antiparasitárias, para aniquilar o parasita, e no controle dos sinais e sintomas da infecção. O tratamento tem como objetivo reduzir a velocidade de acometimento do sistema nervoso parassimpático. Os distúrbios autonômicos provocados pela doença podem resultar, eventualmente, em megaesôfago, megacólon e miocardiopatia dilatada acelerada.
O tratamento antiparasitário é mais eficiente no início da infecção, mas não está limitado à fase aguda. As drogas de escolha incluem os derivados azóis e nitro, tais como o benznidazol38 e o nifurtimox. Ambos os agentes são limitados na sua capacidade de atingir a cura parasitológica (uma eliminação completa do T. cruzi do organismo), especialmente em pacientes cronicamente infectados, e já foram relatados casos de resistência a essas drogas.
Estudos sugerem que o tratamento antiparasitário leva à cura parasitológica em cerca de 60–85% dos adultos e em mais de 90% das crianças tratadas no primeiro ano desde a fase aguda da doença de Chagas. Crianças (idades entre seis e 12 anos) com a doença crônica apresentam uma taxa de cura de aproximadamente 60% com o benznidazol. Apesar de a taxa de cura diminuir com o tempo em que o adulto está infectado com a doença de Chagas, o tratamento com benznidazol tem se mostrado capaz de postergar o início do acometimento cardíaco em adultos com doença de Chagas crônica.17 19
O tratamento da infecção crônica em mulheres antes ou durante a gravidez não parece reduzir a probabilidade de a doença ser transmitida para o bebê. Da mesma forma, não está claro se o tratamento profilático da infecção crônica é benéfico em pessoas que serão submetidas à imunossupressão (por exemplo, em recipientes de transplantes de órgãos) ou em pessoas que já são imunossuprimidas (por exemplo, em pessoas infectadas pelo vírus HIV).
No estado crônico, o tratamento envolve o controle das manifestações clínicas da doença. Por exemplo, marcapassos e medicamentos para arritmias (ritmo irregular dos batimentos cardíacos), como a amiodarona, podem ser muito benéficos para alguns pacientes com acometimento cardíaco crônico, enquanto a cirurgia pode ser necessária no megacólon. Apesar disso, a doença não tem cura nessa fase.
A doença crônica do coração causada pela doença de Chagas tem sido, hoje, uma indicação comum de transplante cardíaco. Até recentemente, contudo, a doença de Chagas era considerada uma contraindicação para esse procedimento, pois acreditava-se que o parasita poderia se aproveitar da imunossupressão após a cirurgia para retomar o acometimento do coração.
Notou-se que as taxas de sobrevida em pacientes com Chagas poderiam aumentar significativamente com a administração de doses menores de drogas imunossupressoras, como a ciclosporina. Recentemente, tem sido demonstrado que o tratamento direto do músculo cardíaco com células-tronco através do transplante de células da medula óssea reduz dramaticamente os riscos de insuficiência cardíaca em pacientes com doença de Chagas.
A doença de Chagas afeta de 8 a 10 milhões de pessoas vivendo em países endêmicos da América Latina, com um adicional de 300 000–400 000 vivendo em países não endêmicos, como Espanha e Estados Unidos. Estima-se que anualmente ocorrem 41 200 novos casos em países endêmicos e que 14 400 crianças nascem com Chagas congênito todos os anos.
Em 2010, a doença resultou em aproximadamente 10 300 mortes em comparação com 9 300 em 1990.43 Estima-se que a taxa de mortalidade anual seja em torno de 14 000.44 No Brasil, estimativas recentes apontam que entre 2 e 3 milhões de pessoas estejam infectadas, e que ocorram cerca de 6 000 mortes anualmente.
A doença está presente em 18 países do continente americano, estendendo-se do sul dos Estados Unidos até o norte da Argentina.2 Chagas existe em duas zonas ecológicas diferentes.
Na região do Cone Sul, o principal vetor vive no interior ou nos arredores das habitações humanas. Na América Central e no México, as principais espécies vetoras vivem tanto no interior das casas como em áreas desabitadas. Em ambas as zonas, a doença de Chagas ocorre quase exclusivamente em áreas rurais, onde os triatomíneos procriam e se alimentam das mais de 150 espécies de 24 famílias de mamíferos domésticos e selvagens, bem como de humanos, que servem de reservatórios naturais do T. cruzi.
Embora os triatomíneos também se alimentem do sangue de pássaros, estes parecem ser imunes à infecção e não são considerados reservatórios do T. cruzi. Mesmo quando colônias de insetos são erradicadas de uma casa ou de abrigos de animais nas redondezas, eles podem re-emergir de plantas ou animais que fizeram parte do ciclo silvático (referente a animais selvagens) do parasita. Esse fenômeno é especialmente provável em zonas com vegetações abertas misturadas a agrupamentos de árvores e interpostas por habitações humanas.
A doença de Chagas crônica permanece um importante problema de saúde pública em muitos países da América Latina, apesar das medidas efetivas de higiene e prevenção, como a eliminação dos insetos transmissores.
Entretanto, algumas conquistas foram alcançadas na luta contra a doença na América Latina, como a redução de 72% da incidência da infecção em crianças e adultos jovens nos países da Iniciativa do Cone Sul e pelo menos três países (Uruguai, em 1997, Chile, em 1999, e Brasil, em 2006) foram certificados como livres da transmissão vetorial e transfusional.
Na Argentina, a transmissão vetorial foi interrompida em 13 das 19 províncias endêmicas e progressos significativos têm sido feitos nesse sentido no Paraguai e na Bolívia.48
O monitoramento para T. cruzi do sangue doado e dos doadores de componentes sanguíneos e de órgãos sólidos, assim como dos doadores de células, tecidos e produtos de células e tecidos, é mandatório nos países endêmicos de Chagas e tem sido implementado.
Com o aumento dos movimentos populacionais, a possibilidade de transmissão por transfusão de sangue se tornou mais substancial nos Estados Unidos. A transfusão de sangue e produtos de tecidos é ativamente monitorada nos Estados Unidos, diminuindo, portanto, o risco.
Veja na Rua Direita



















 Ajude-nos a manter o site actualizado
Ajude-nos a manter o site actualizado